|
|
[回上頁 | 顯示此文件為可列印格式]
此文件提供者: agrkb - [評分 : 0.00 (0 票選) | 評分!]
生殖細胞的冷凍 45 第二章
精子銀行 |
玖、鹽化豬卵供測試家畜禽精子受精力
豬卵巢濾泡中的卵丘卵母細胞複合體經鹽化保存於冰箱,直至使用前才予以脫鹽和去除卵丘細胞層,使卵透明帶裸露。脫鹽後的豬卵每15個放入一培養小滴,每一培養皿內有兩個培養小滴。稀釋後精液再置放入這兩個培養小滴,使之和卵混合,蓋上礦物油的培養小滴於39℃恆溫培養箱中培養15小時。粘附在豬卵透明帶外的多餘精子經反覆沖吸方式洗掉,再把豬卵螢光染色,鏡檢透明帶上的精子數。有五頭紐西蘭白兔、五隻土雞、四隻菜鴨和九隻正番鴨的新鮮精液,一頭老鼠的附睪尾部精液,以及有七頭荷蘭乳牛、四頭台灣水牛和四隻中國鵝的冷凍精液被測試。在鏡檢的1540個豬卵記錄裡,單一豬卵透明帶中能被乳牛、水牛、兔、雞、菜鴨、正番鴨、鵝、老鼠等之精子鑽入最多的精子數分別有69、118、15、42、39、59、13、0個精子。當比較同品種不同個體精液之精子鑽入豬卵透明帶的比率或卵透明帶中的精子數,均顯示有種公畜個體差異存在。老鼠精子雖可粘附在鹽化豬卵的透明帶上,但並未鑽入。因此,以鹽化豬卵來測試其他家畜禽精子之鑽入透明帶的能力是有其潛在用途。
受精力評估
哺乳動物的精子和卵之結合,端賴精子是否有能力去粘附於卵丘細胞層、去穿入透明帶、去通過卵細胞膜、以及產生原核融合等系列性步驟。因此,哺乳動物精子的受精力評估方式一直是繁殖管理者所企求的。應用體外受精系統來檢測精卵結合狀態及其爾後的胚發育是目前普遍被接受的方式,可是獲取新鮮卵或冷凍卵的體外培養方式又費時費力,尤其是排卵數少的單胎動物,不僅卵的取得困難而且費用昂貴。Yanagimachi (1972)和
Yanagimachi et al.(1976)就進行倉鼠卵供其他物種和人之精子受精能力鑑定試驗,顯示倉鼠卵是人精子受精力鑑定的替代性卵。並於1979年又證實倉鼠卵和人卵鹽化保存後仍保有完整的透明帶且可讓精子去粘附和穿透的特性(Yanagimachi et al., 1979)。
透明帶醣蛋白
豬卵透明帶厚度約有16um和含有30~35ng蛋白質(Dunbar, 1983)。豬透明帶的醣蛋白是酸性醣蛋白,經加熱至70℃數分鐘後,可被軟化而熔解開,依其分子量大小而有ZP1、ZP2和ZP3(Nakano et al., 1987a)。豬ZP1在受精時會被進一步分切成碳端醣蛋白的ZP2和氮端醣蛋白的ZP4兩部份
|
生殖細胞的冷凍 46 第二章
精子銀行 |
| (Hedrick et
al., 1987; Hatanaka et al., 1992)。因此,豬ZP1易受蛋白酵素(Proteases)分解,而ZP3不易(Nakano et al.,
1987b, 1989)。由於ZP3的胺基結構不會和螢光染色劑FITC(Fluorescein isothiocyanate)結合,但ZP1的胺基會和FITC結合,所以透過螢光染色法,證實ZP1是分布於豬卵透明帶的外層,而ZP3則分布於內層(Hatanaka et al., 1988)。根據Harris et
al.(1994)和Hedrick (1996)在人和鼠卵透明帶醣蛋白基因研究文獻檢討裡,指出透明帶醣蛋白基因有三,並依基因序列大小分類為ZPA、ZPB和ZPC基因,其基因產物依序為ZP2、ZP1和ZP3。但豬的ZPA基因產物是ZP1,而其分解物為ZP2和ZP4;至於豬ZPB和ZPC基因產物則分別是ZP3的alpha鏈和beta鏈。
頭帽反應
頭帽完整的小鼠精子會先和透明帶上的ZP3結合,而產生頭帽反應(Bleil and Wassarman, 1983)。穿入透明帶且已有頭帽反應的小鼠精子會和其中的ZP2結合,待首批精子通過透明帶後,其透明帶會發生硬化現象(Zona hardening),阻止其他精子的繼續穿透,達到防止多精入卵的效果(Bleil et al., 1988; Moller and Wassarman,
1989)。豬卵透明帶上的各類醣蛋白均可和精子粘合,並誘發豬精子的頭帽反應(Berger et al., 1989a,b; Yurewicz et al.,
1991; Fierro et al., 1994)。不過,豬和牛的受精過程裡以卵透明帶的ZP1和有頭帽反應的精子一結合後,就會促使透明帶有硬化現象,以阻止多精入卵(Hatanaka et al., 1992; Noguchi et al.,
1994)。根據Zhang et al.(1995)以新鮮牛卵進行透明帶上精子穿透數和牛卵體外受精後受精卵數之相關分析,發現每15個卵為一鑑定單位時,卵的個別差異性之影響性可被減至最低。Cox(1992)利用有卵丘細胞包被著的牛卵、綿羊卵、豬卵和小鼠卵來測試已獲能作用的乳牛精子,發現13.2%的豬卵透明帶上鑽有乳牛精子,而僅有0.8%的豬卵細胞質中有牛精子鑽進,顯示豬卵透明帶可供鑑別乳牛精子穿透透明帶能力用。
溶液組成分
速保精(Sperm-up)溶液 500毫升瓶裝者,內含
33 g Dextrose monohydrate、1.85g Sodium citrate dihydrate、 1.85 g EDTA 、 0.8 g Sodium bicarbonate、250 mg Ampicillin sodium 和250 mg
Dihydrostreptomycin sulfate。鹽化豬卵的鹽漬液是
1.5 M MgCl2•6H2O、0.1% Polyvinylpyrrolidone (PVP)和 40 mM HEPES 配製而成並調整為 pH = 7.2。螢光染色劑溶液是在每毫升速保棈溶液加入 SYBR-14和 Propidium iodide備用溶液各
20ul。SYBR-14和Propidium iodide染色套組取自FertiLight商品名(Molecular Probes, Inc., Eugene, OR, USA),該染色套組專供檢測活的、垂死的和死的精子,在
|
生殖細胞的冷凍 47 第二章
精子銀行 |
| 488nm波長下活的精子呈綠螢光,垂死的精子呈黃螢光,而死的精子呈紅螢光(Garner and Johnson, 1995)。
鹽化豬卵
臺灣養豬事業發達,屠宰母豬的卵巢含有10個以上的未成熟卵可加以回收。因此,仿照倉鼠卵和人卵的鹽化方式,把豬卵先鹽化。經鹽化的豬卵可否做為其他動物的精子鑽入透明帶能力之鑑定用,是本研究的目的。卵之準備上,從電宰肉豬回收的卵巢先經速保精溶液洗滌三次後,再以解剖刀的刀尖來刺破卵巢上的濾泡,以之回收濾泡內的卵丘卵母細胞複合體。仿照吳等(1996)在鹽化豬卵應用於豬精子的穿透力鑑定研究所述,把卵丘卵母細胞複合體再經速保精溶液洗滌一次後,就直接放入鹽化溶液,置於
6℃
冰箱保存一夜,製成鹽化豬卵。鹽化豬卵使用前再以速保精溶液來洗滌,藉以去除鹽漬液和包圍在透明帶外的卵丘細胞,使卵透明帶裸露。經脫鹽清洗後的每批豬卵,先逢機選取其中的5%的卵,先以豬精子混合培養15小時,確定這些脫鹽卵透明帶能被豬精子鑽入,才供其他物種之精子測試用。
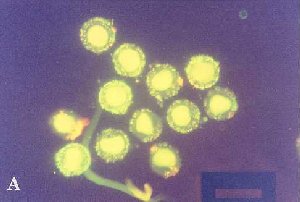 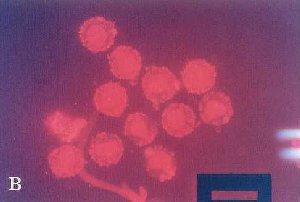
在可見波長488 nm (A)和546 nm (B)螢光鏡檢
豬精子鑽入豬卵透明帶狀況。x100。
|
生殖細胞的冷凍 48 第二章
精子銀行 |
| 精子鑽入透明帶測試
五頭紐西蘭白兔、五隻土雞、四隻菜鴨和九隻正番鴨的新鮮精液,以及七頭荷蘭乳牛、四頭台灣水牛和四隻中國鵝的冷凍精液。新鮮精液以速保精(中化製藥,台北)
溶液稀釋兩倍,藉以減低精子濃度。冷凍精液各按其解凍步驟至可供人工授精用濃度,就直接取用。一頭老鼠的附睪精子是取自成熟老鼠的附睪尾。
鹽化豬卵 15個放入100μl的速保精溶液小滴,每一培養皿內置兩小滴,合計30個卵為一鑑定用單位。測試時先取10μl精液放入培養皿的其中一小滴,再取100μl精液放入另一小滴,然後以礦物油覆蓋兩小滴。在39℃恆溫培養箱予以共培養15小時後,卵被吸出培養小滴並以速保精溶液反覆沖洗洗滌三次以上,去除粘附在透明帶外的多餘精子。再把這些卵放入25μl的螢光染色劑小滴,就可在可見光波長488
nm 或 546 nm 清晰看到有多少精子鑽在透明帶裡。
新鮮豬卵經去除卵丘細胞後成為裸露透明帶的豬卵,使用兩頭荷蘭乳牛冷凍精液來進行精子鑽入測試,且把同一頭乳牛精液亦以鹽化豬卵進行精子鑽入測試。一頭老鼠的附睪尾部以速保精溶液浸泡並擠出其內的精液,就取樣放入新鮮豬卵和鹽化豬卵,進行精子鑽入透明帶測試。
荷蘭乳牛、台灣水牛、台灣土雞、菜鴨、中國鵝、紐西蘭白兔、正番鴨和老鼠等家畜禽精子鑽在鹽化豬卵透明帶的精子數列於表。荷蘭乳牛和台灣水牛的解凍精液之精子濃度相似,但台灣水牛精子鑽在豬卵透明帶上的精子數很多,最多者有118
個精子鑽在一個卵透明帶上。由於牛卵取得不易,故本研究以豬卵替代時,亦能鑑別個別牛隻精子鑽入透明帶之差異,甚至種別間之不同。早期研究中,直接回收已冷凍的母牛卵巢,把冷凍卵巢內的卵再回收,做為牛精子穿透力鑑定用,亦有如新鮮卵有效(Wheeler and Seidel, 1987,1989; Tatemoto et al.,
1994)。自冷凍的豬卵巢回收其內的卵,再被用來鑑定豬精子穿透力試驗,已在1978年就進行過(Downey et al., 1978)。利用不同物種的卵來鑑別精子粘附和穿透能力之研究上,或可大量回收已冷凍的豬卵巢或未冷凍的豬卵巢,再把其內的卵予以鹽化,進而提供給牛精子受精力鑑定用,是一項待研發的技術。
|
生殖細胞的冷凍 49 第二章
精子銀行 |
家畜精子鑽入鹽化豬卵透明帶的精子數 |
動物類別 |
代碼 |
受測卵數 |
被鑽入的卵數(%) |
依卵透明帶上被鑽入的精子數分類(最高精子數者) |
1~5 |
6~30 |
>30 |
荷蘭乳牛 |
H1 |
30 |
20( 66.7) |
14 |
5 |
1(46) |
H2 |
30 |
30(100.0) |
0 |
2 |
28(69) |
H3 |
30 |
30(100.0) |
6 |
12 |
12(57) |
H4 |
30 |
30(100.0) |
0 |
0 |
30(58) |
H5 |
30 |
16( 53.3) |
2 |
0 |
14(37) |
台灣水牛 |
TWB1 |
30 |
28( 93.3) |
7 |
9 |
12(118) |
TWB2 |
15 |
15(100.0) |
1 |
4 |
10(65) |
TWB3 |
30 |
30(100.0) |
8 |
10 |
12(62) |
TWB4 |
30 |
30(100.0) |
4 |
11 |
15(73) |
紐西蘭白兔 |
NZW1 |
30 |
0( 0.0) |
0 |
0 |
0 |
NZW2 |
30 |
0( 0.0) |
0 |
0 |
0 |
NZW3 |
30 |
3( 10.0) |
3(2) |
0 |
0 |
NZW4 |
30 |
5 (16.7) |
5(4) |
0 |
0 |
NZW5 |
90 |
33(36.7) |
30 |
3(15) |
0 |
乳牛精子鑽入新鮮豬卵和鹽化豬卵透明帶之比較 |
荷蘭乳公牛 |
豬卵 |
受測卵數 |
被鑽入的卵數(%) |
依卵透明帶上被鑽入的精子數分類及其所佔百分比 |
1~5 |
6~30 |
>30 |
H6 |
新鮮豬卵 |
161 |
132( 82.0) |
85(64.4) |
44(33.3) |
3( 2.3) |
鹽化豬卵 |
99 |
56( 56.6) |
39(69.6) |
14(25.0) |
3( 5.4) |
H7 |
新鮮豬卵 |
30 |
30(100.0) |
6(20.0) |
16(53.3) |
8(26.7) |
鹽化豬卵 |
30 |
30(100.0) |
0( 0.0) |
3(10.0) |
27(90.0) |
|
| 生殖細胞的冷凍 50 第二章
精子銀行 |
家禽精子鑽入鹽化豬卵透明帶的精子數 |
動物類別 |
代碼 |
受測卵數 |
被鑽入的卵數(%) |
依卵透明帶上被鑽入的精子數分類(最高精子數者) |
1~5 |
6~30 |
>30 |
台灣土雞 |
TNC1 |
30 |
19( 63.3) |
14 |
4 |
1(37) |
TNC2 |
28 |
16( 57.1) |
10 |
4 |
2(42) |
TNC3 |
27 |
17( 63.0) |
9 |
0 |
8(35) |
TNC4 |
30 |
14( 46.7) |
9 |
1 |
4(39) |
TNC5 |
30 |
14( 46.7) |
10 |
3 |
1(32) |
菜鴨 |
TD1 |
30 |
14( 46.7) |
9 |
4 |
1(39) |
TD2 |
29 |
20( 69.0) |
16 |
3 |
1(35) |
TD3 |
28 |
19( 67.9) |
16 |
3(10) |
0 |
TD4 |
27 |
20( 74.1) |
15 |
4 |
1(35) |
正番鴨 |
MD1 |
90 |
0( 0.0) |
0 |
0 |
0 |
MD2 |
30 |
0( 0.0) |
0 |
0 |
0 |
MD3 |
30 |
0( 0.0) |
0 |
0 |
0 |
MD4 |
30 |
12( 40.0) |
11 |
1(8) |
0 |
MD5 |
30 |
6( 20.0) |
4 |
2(17) |
0 |
MD6 |
30 |
14( 46.7) |
4 |
8 |
2(35) |
MD7 |
30 |
8( 26.7) |
1 |
0 |
7(59) |
MD8 |
30 |
7( 23.3) |
0 |
6 |
1(31) |
MD9 |
24 |
14( 58.3) |
11 |
1 |
2(35) |
中國鵝 |
CG1 |
22 |
7( 31.8) |
6 |
1(13) |
0 |
CG2 |
30 |
0( 0.0) |
0 |
0 |
0 |
CG3 |
30 |
2( 6.7) |
2(1) |
0 |
0 |
CG4 |
30 |
29( 96.7) |
29(1) |
0 |
0 |
|
生殖細胞的冷凍 51 第二章
精子銀行 |
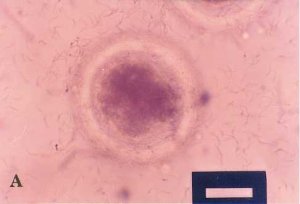 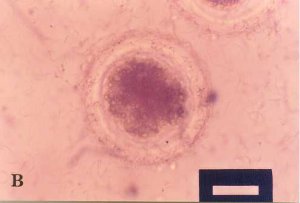
正番鴨精子粘附在豬卵透明帶。A圖對焦在卵面上方,
B圖對焦在卵中央。x400。
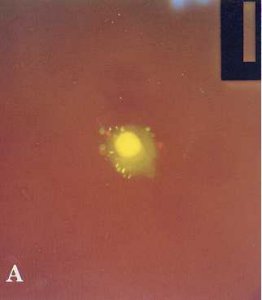 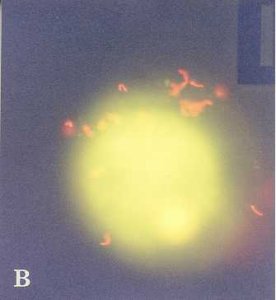
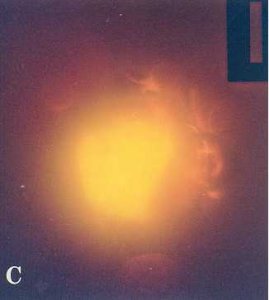 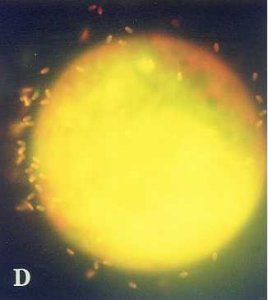
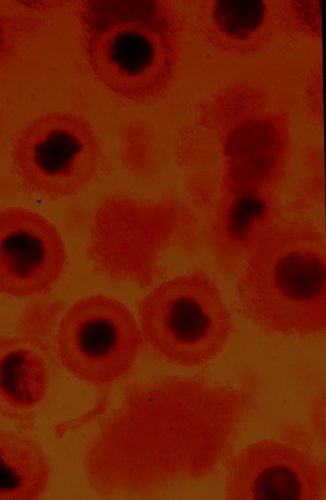
螢光鏡檢鵝(A)、雞(B)、菜鴨(C)和水牛精子(D)鑽入豬卵透明帶
狀況。鏡檢倍數分別為x100、x400、x400和x1000。波長為488nm。
|
生殖細胞的冷凍 52 第二章
精子銀行 |
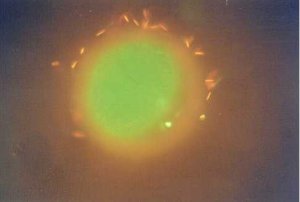 
螢光鏡檢乳牛精子粘附在(左圖)和鑽入(右圖)新鮮
且先去除卵丘細胞的豬卵透明帶。X320。
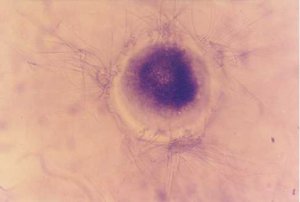 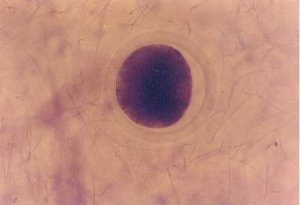
老鼠精子可粘附在鹽化豬卵透明帶(左圖),但不粘附在去
卵丘細胞的新鮮豬卵透明帶(右圖)。
X400。
|
生殖細胞的冷凍 53 第二章
精子銀行 |
| 豬透明帶醣蛋白ZP1
鹽化豬卵透明帶能被牛、兔、雞、鴨、鵝精子的粘附,進而鑽入在透明帶的試驗結果,說明其透明帶的結構物醣蛋白ZP1和ZP3可能仍具生物活性。ZP3是和精子粘附的主要醣蛋白(Wassarman,
1990);而ZP2是由ZP1分解而來的,其功能是給有頭帽反應精子粘附的次要醣蛋白(Hasegawa
et al., 1994)。Tsubamoto et al.(1996)更應用豬透明帶醣蛋白ZP1的基因序列,透過大腸桿菌來遺傳工程合成有198個胺基酸組成的氮端醣蛋白r-pZP1(198)。該作者把這種醣蛋白和豬、人、兔、天竺鼠和小鼠等五種已有頭帽反應的精子一起共培養18小時後,發現粘附的位置可由精子的頭、頸至尾部逐漸擴大,證實了豬卵透明帶其有讓其他種動物精子粘附的結構,並進而可促使粘附精子去穿入透明帶。
精子鑽入率
五頭紐西蘭白兔有個體差異存在,其中兩頭的精子均未鑽入卵透明帶(0/60);其他三頭的精子鑽入了
10~ 37﹪的卵透明帶,其鑽入的精子數最多者為15。土雞精子鑽入卵透明帶的百分率,介於47~63﹪不等,鑽入的精子數最多有
42。菜鴨精子鑽入了 47~74﹪的卵,鑽入的精子數最多有39。九隻正番鴨亦有個體差異,每隻正番鴨的精子均可粘附在豬卵透明帶,且數量很多,但洗滌後有三隻正番鴨的精子均未鑽入任何一個卵的透明帶(0/150),另六隻正番鴨的精子鑽入了
20~58% 的卵,鑽入的精子數最多者有59。鵝精子鑽入了6.7~19.7﹪的卵,鑽入的精子數最多有 13。雞、菜鴨和水牛精子鑽入豬卵透明帶,但大多數精子已呈現紅螢光,而鵝精子仍呈現綠螢光。Lassalle and Testart (1996)研究人精子和卵受精過程中,發現人精子一鑽入卵透明帶就會發生精子的頭帽反應,導致細胞膜裂損,於螢光顯微鏡觀察下,逐漸由綠螢光轉成紅螢光。因此,本研究中呈現綠螢光的精子,可被推測是仍保有完整的細胞膜尚未產生頭帽反應的精子。
Yanagimachi(1981)明確地指出哺乳動物的精子,需具有粘附在卵透明帶的能力,始能進而穿透透明帶,完成精卵結合的受精目的。牛、兔、雞、鴨、鵝精子能粘附且能鑽入豬卵透明帶,但兔和鵝精子鑽入數較少,同時個體間有差異,暗示精子粘附和鑽入之間可能涉及精子頭帽反應程度。豬、小鼠和人精子的頭帽反應是粘附在透明帶後才開始
(Wassarman, 1988 ; Liu and Baker, 1990 ;
Yoshizawa et al . ,1994),而天竺鼠精子先有頭帽反應才能粘附透明帶(Yangaimachi, 1981) 。豬卵透明帶是卵細胞外圍的包被物質,扮演精卵受精過程中極為主要的角色,不僅涉及有種別性的精卵粘附作用,尚涉及精子頭帽反應的誘發和卵受精後阻斷多餘精子的穿入(Wassarman, 1990)。雖
|
| 生殖細胞的冷凍 54 第二章
精子銀行 |
| 然O'Rand(1988)認為兩種不同種動物的精卵結合之最大障礙是卵透明帶,但Slavik et al.(1990)和Cox(1992)均認為草食獸間不明顯,綿羊精子易穿入牛卵透明帶,而牛精子亦可穿入綿羊卵透明帶。不過Cox(1992)把不同物種的精子和卵進行異種間體外受精時,把受精後的精子區分為三種狀態:僅粘附在透明帶外層上、鑽入透明帶、和鑽進卵細胞質等。他利用有卵丘細胞包被著的牛卵、綿羊卵、豬卵和小鼠卵來測已獲能作用後的乳牛精子,得到77.1%(27/35)、46.0%(23/50)、13.2%(16/121)、和0.0%(0/80)的上述物種的卵透明帶被乳牛精子鑽入,但有97.1%(33/34)、93.9%(46/49)、0.8%(1/121)Co和0.0%(0/80)的卵細胞質中有鑽進的乳牛精子。他認為乳牛精子不易穿透豬卵透明帶而鑽進細胞質中,是因為物種的差異。若僅以精子鑽入透明帶來看時,在Cox(1992)之研究中得到13.2%的新鮮豬卵透明帶能被乳牛精子鑽入,而五頭荷蘭乳牛和四頭台灣水牛之精子穿入鹽化後豬卵透明帶的百分比大於53.3%,顯有不同之處。一者本研究所使用的鹽化豬卵已去除卵丘細胞,二者Cox氏所用的乳牛精子濃度為0.6×106精子/ml,而本研究所使用的精子濃度較高,有10×106精子/ml。當我們進一步比較鹽化豬卵和去除卵丘細胞後的新鮮豬卵授于相同一隻牛精液後,再檢測精子鑽入透明帶狀況,其結果列於表。就新鮮卵和鹽化卵被精子鑽入的卵數百分率來看,兩頭乳牛精子有個體差異,但精子鑽入鹽化豬卵的百分率以多於30隻精子數比較時,較新鮮豬卵者為多。豬卵經鹽化後再脫鹽去卵丘細胞的30個鹽化卵,與去卵丘細胞的30個新鮮卵被用來初步檢試老鼠精子的鑽入透明帶能力時,發現老鼠精子可粘附在鹽化豬卵透明帶上,但無法粘附在新鮮卵透明帶。當把有老鼠精子粘附的鹽化豬卵經三次吸放的洗滌後,30個鹽化豬卵在螢光鏡檢下並未發現有精子,顯示老鼠精子並未鑽入鹽化豬卵透明帶。有關此項差異,將另行設計試驗,進行老鼠精子粘附或鑽入豬卵的後續試驗。
鑑定用卵之取得
Cox et al.(1994)更進一步證實山羊精子可不受牛卵和綿羊卵外圍包被著的卵丘細胞,影響到其穿入兩者卵透明帶的能力。這些參考文獻所進行的檢測試驗均以新鮮卵為鑑定卵,但已顯示精子穿入透明帶能力,在牛羊間並無種別性之考量。但若以牛卵和羊卵來鑑定草食獸精子時,其卵的來源在台灣地區似不如豬卵。由於使用同一物種的卵來進行精子穿透力鑑定,對人和牛等單胎動物和鳥類有先天上的不便。倉鼠卵被用作人(Yanagimachi,1972; Yanagimachi et al., 1976;
Overstreet et al., 1980; Yanagimachi, 1984)和貓精子 (Goodrowe and Hay,
1993)的穿透力鑑定時,需回收體內成熟的卵並需去除透明帶後才能被使用,亦有所不便。
|
生殖細胞的冷凍 55 第二章
精子銀行 |
| 不同的鹽化液
本研究採用近似 Yanagimachi et al. (1979)用來鹽漬小鼠卵的鹽漬溶液(1.5M MgCl2+0.1﹪PVP)。該小鼠卵鹽漬液被 Kruger et al.(1991)再添加40mM HEPES
後,用於人卵的鹽化用,發現鹽化卵和新鮮卵具有相同的粘附精子能力。雖然
Fazeli et al.(1995)亦用來鹽漬豬卵,但他們認為另一種鹽漬溶液(2M (NH4)2SO4+0.5﹪Dextran+40mH HEPES, pH=7.0)較適宜於鑑定公豬受精力。早在1979年,Yanagimachi et al. 就以2M (NH4)2SO4和0.1﹪ Dextran
來鹽漬豬卵,隨後用來和人精子混合,人精子並未穿入豬卵透明帶。由於Tsubamoto et al.(1996)已證實有頭帽反應的人精子易於粘附於豬透明帶的ZP1醣蛋白,可見不同的鹽化液會影響到卵透明帶醣蛋白的粘附精子之能力。鹽化豬卵的製備和使用上均簡易可行,將有助於人精子和其他動物精子之穿透力鑑定普遍化,亦可藉此建立雄性受精力指數。
參考文獻
吳明哲、李秀美、劉振發、周佳樂、高瑞娟。1996。應用鹽化豬卵進行公豬受精力之鑑定。中畜會誌
25(增刊): 68。
Berger, T., A. Davis, N. J. Wardrip and J. L.
Hedrick. 1989a. Sperm binding to the pig zona pellucida and inhibition of binding by
solubilized components of the zona pellucida. J. Reprod. Fertil. 86: 559-565.
Berger, T., K. G. Turner, S. Meizel and J. L.
Hedrick. 1989b. Zona pellucida-induced acrosome reaction in boar sperm. Biol. Reprod.
40: 525-530.
Bleil, L. D. and P. M. Wassarman. 1983. Sperm-egg
interactions in the mouse: Sequence of events and induction of the acrosome reaction by a zona
pellucida glycoprotein. Develop. Biol. 95: 317-324.
Bleil, J. D., J. M. Greve and P. M. Wassarman.
1988. Identification of a secondary sperm receptor in the mouse egg zona pellucida: Role
in maintenance of binding of acrosome-reacted sperm to eggs. Develop. Biol. 128: 376-385.
Cox, J. F. 1992. Heterologous fertilization using
livestock gametes. Arch. Med. Vet. 24: 25-31.
Cox, J. F., A. Catalan, F. Saravia, J. Avila and
A. Santa Maria. 1994. In vitro fertilization of cattle and sheep follicular oocytes by
goat spermatozoa. Small Ruminant Res. 15: 55-58.
Downey, B. R., N. B. Segal and R. D. Baker. 1978.
Sperm penetration of live and dead oocytes within oviducts of gilts. Can. J. Anim. Sci.
58: 339-344.
|
| 生殖細胞的冷凍 56 第二章
精子銀行 |
| Dunbar, B. S. 1983.
Morphological, biochemical, and immunochemical characterization of the mammalian zona pellucida. In
Mechanism and Control of Animal Fertilization. (J. F. Hartmann, ed.). Academic
Press, New York. pp.139-175.
Fazeli, A. R., C. Holt, W. Steenweg, M. M.
Bevers, W. V. Holt and B. Colenbrander. 1995. Development of a sperm hemizona binding
assay for boar semen. Theriogenology 44: 17-27.
Fierro, R., E. Bonilla, E. Casas, I. Jimenez, Y.
Ducolomb and M. Betancourt. 1994. Inhibition of pig oocyte in vitro fertilization by the
action of components of the zona pellucida. Theriogenology 42: 227-234.
Garner, D. L. and L. A. Johnson. 1995. Viability
assessment of mammalian sperm using SYBR-14 and propidium iodide. Biol Reprod. 53:
276-284.
Goodrowe, K. L. and M. Hay. 1993. Characteristics
and zona binding ability of fresh and cooled domestic cat epididymal spermatozoa.
Theriogenology 40:967-975.
Harris, J. D., D. W. Hibler, G. K. Fontenot, K.
T. Hsu, E. C. Yurewicz and A. G. Sacco. 1994. Cloning and characterization of zona pellucida genes
and cDNA from a variety of mamalian species: the ZPA, ZPB and ZPC gene families. DNA
Sequence- J. Sequencing Mapping 4: 361-393.
Hasegawa, A., K. Koyama, Y. Okazaki, M. Sugimoto
and S. Isojima. 1994. Amino acid sequence of a porcine zona pellucida glycoprotein ZP4
determined by peptide mapping and cDNA cloning. J. Reprod. Fertil. 100: 245-255.
Hatanaka, Y., M. Nakano and T. Tobita. 1988.
Modification of porcine zona pellucida with fluorescein isothiocyanate: Evidence for the
presence of a structural unit consisting of glycoproteins in the mammalian egg coat.
Biochem. Intl. 17: 935-944.
Hatanaka, Y., T. Nagai, T. Tobita and M. Nakano.
1992. Changes in the properties and composition of zona pellucida of pigs during
fertilization in vitro. J. Reprod. Fertil. 95: 431-440.
Hedrick, J. L. 1996. Comparative structural and
antigenic properties of zona pellucida glycoproteins. J. Reprod. Fertil., Suppl. 50: 9-17.
Hedrick, J. L., N. J. Wardrip and T. Berger.
1987. Differences in the macromolecular composition of the zona pellucida isolated from
pig oocytes, eggs, and zygotes. J. Expt. Zoology 241: 257-262.
|
生殖細胞的冷凍 57 第二章
精子銀行 |
| Kruger, T.
F., S. Oehninger, D. R. Franken and G. D. Hodgen. 1991. Hemizona assay: Use of fresh
versus salt-stored human oocytes to evaluate sperm binding potential to the zona
pellucida. J. Intl. Vitro Fertil. Embryo Transfer 8: 154-156.
Lassalle, B. and J. Testart. 1996. Lectins
binding on human sperm surface increase membrane permeability and stimulate acrosomal
exocytosis. Mol. Human Reprod. 2(9): 651-658.
Liu, D. Y. and H. W. G. Baker. 1990. Inducing the
human acrosome reaction with a calcium ionophore A23187 decreases sperm-zona pellucida
binding with oocytes that failed to fertilize in vitro. J. Reprod. Fertil. 89: 127-134.
Nakano, M. Y. Hatanaka, T. Sawai, N. Kobayashi
and T. Tobita. 1987a. Fractionation of glycoproteins from porcine zonae pellucidae into
three families by high-performance liquid chromatography. Biochem. Intl. 14: 417-423.
Nakano, M., Y. Hatanaka and T. Tobita. 1987b.
Solubilization of porcine zonae pellucidae by trypsin and pronase. Biochem. Intl. 14:
425-433.
Nakano, M., Y. Tanaka, T. Kimura, Y. Hatanaka and
T. Tobita. 1989. Boar acrosin digestion of the porcine egg coat, zona pellucida, and
rearrangement of the zona proteins. J. Biochem. (Tokyo) 105: 138-142.
Noguchi, S., N. Yonezawa, T. Katsumata, K.
Hashizume, M. Kuwayama, S. Hamano, S. Watanabe and M. Nakano. 1994. Characterization of
the zona pellucida glycoproteins from bovine ovarian and fertilized eggs. Biochimica et Biophysica Acta
1201: 7-14.
O'Rand, M. G. 1988. Sperm recognition and
barriers to inter-species fertilization. Gamete Res. 19: 315-328.
Overstreet, J.W., R. Yanagimachi, D. F. Katz, K.
Hayashi and F. W. Hanson. 1980. Penetration of human spermatozoa into the human zona
pellucida and the zona-free hamster egg: A study of fertile donors and infertile patients.
Fertil. Steril. 33: 534-542.
Slavik, T., A. Pavlok and J. Fulka. 1990
Penetration of intact bovine ova with ram sperm in vitro. Mol. Reprod. Dev. 25: 345-347.
Tatemoto, H., T. Horiuchi, T. Maeda, T. Terada
and Y. Tsutsumi. 1994. Penetration by bull spermatozoa into the zona pellucida of dead bovine oocytes
recovered from frozen-thawed ovaries. Theriogenology 42: 465-474.
|
生殖細胞的冷凍 58 第二章
精子銀行 |
| Tsubamoto,
H., A. Hasegawa, M. Inoue, N. Yamasaki and K. Koyama. 1996. Binding of recombinant pig
zona pellucida protein 1 (ZP1) to acrosome-reacted spermatozoa. J. Reprod. Fertil., Suppl.
50: 63-67.
Wassarman, P. M. 1988. Zona pellucida
glycoproteins. Ann. Rev. Biochem. 57: 415-442.
Wassarman, P. M. 1990. Profile of a mammalian
sperm receptor. Development 108: 1-17.
Wheeler, M. B. and G. E. Jr. Seidel. 1987. Zona
pellucida penetration assay for capacitation of bovine sperm. Gamete Res. 18: 237-250.
Wheeler, M. B. and G. E. Jr. Seidel. 1989.
Capacitation of bovine spermatozoa by lysophospholipids and trypsin. Gamete Res. 22:
193-204.
Wu, M. C. and H. M. Lee. 1996. Vitrification of
porcine oocytes. J. Chin. Soc. Anim. Sci. 25(1): 35-51.
Yanagimachi, R. 1972. Penetration of guinea-pig
spermatozoa into hamster eggs in vitro. J. Reprod. Fertil. 28: 477-480.
Yanagimachi, R. 1981. Mechanisms of fertilization
in mammals. In Fertilization and Embryonic Development in Vitro (L. Mastroianni and
J. D. Biggers, eds.). Plenum Press, New York. pp. 81-182.
Yanagimachi, R. 1984. Zona-free hamster eggs:
Their use in assessing fertilizing capacity and examining chromosomes of human
spermatozoa. Gamete Res. 10: 187-232.
Yanagimachi, R., H. Yanagimachi, B. J. Rogers.
1976. The use of zona-free animal ova as a test-system for the assessment of fertilizing
capacity of human spermatozoa. Biol. Reprod. 15: 471-476.
Yanagimachi, R., A. Lopata, C. B. Odom, R. A.
Bronson, C. A. Mahi and G. L. Nicolson. 1979. Retention of biologic characteristics of
zona pellucida in ighly concentrated salt solution: The use of salt-stored eggs for
assessing the fertilizing capacity of spermatozoa. Fertil. Steril. 31: 562-574.
Yoshizawa, M., T. Nagai, N. Yonezawa and M.
Nakano. 1994. Native zona pellucida structure is required for completion of sperm acrosome
reaction in porcine fertilization. Theriogenology 41: 1307-1313.
Yurewicz, E. C., B. A. Pack and A. G. Sacco.
1991. Isolation, composition, and biological activity of sugar chains of porcine zona
pellucida 55K glycoproteins. Mol. Reprod. Develop. 30: 126-134.
|
生殖細胞的冷凍 59 第二章
精子銀行 |
| Zhang, B.
R., B. Larsson and H. Rodriguezmartinez. 1995. Influence of batches of bovine oocytes on
the outcome of an intact zona-pellucida binding assay and in-vitro fertilization. Intl. J.
Andrology 18(4): 213-220.
|
[回上頁 | 顯示此文件為可列印格式]
此文件提供者: agrkb - [評分 : 0.00 (0 票選) | 評分!]
|
|
| 所徽 |
|

|
| 隨機小語 |
一個國家偉不偉大、道德水準高不高可以從它對待動物的方式評斷出來。
[甘地] |
|